
- Pengarang Miles Stephen stephen@answers-science.com.
- Public 2023-12-15 23:39.
- Diubah suai terakhir 2025-01-22 17:06.
Jika anda perlu guna ini persamaan , cuma cari butang "ln" pada kalkulator anda. Awak boleh gunakan persamaan Arrhenius untuk menunjukkan kesan perubahan suhu pada pemalar kadar - dan oleh itu pada kadar tindak balas. Jika pemalar kadar meningkat dua kali ganda, sebagai contoh, kadar tindak balas juga akan berlaku.
Begitu juga, apakah formula untuk tenaga pengaktifan?
Menentukan Tenaga Pengaktifan. Perhatikan bahawa apabila persamaan Arrhenius disusun semula seperti di atas, ia adalah persamaan linear dengan bentuk y = mx + b; y ialah ln(k), x ialah 1/T, dan m ialah -Ea/R. Tenaga pengaktifan untuk tindak balas boleh ditentukan dengan mencari cerun daripada barisan.
Selain itu, apakah unit untuk K? Daripada corak unit kita boleh menyatakan bahawa untuk tindak balas tertib kinetik n, the unit daripada k ialah: k = 1/tc^(n-1), mengingati bahawa c ialah jumlah seliter yang dinyatakan dalam jisim atau kemolaran dan n ialah tertib kinetik.
Kemudian, apakah unit tenaga pengaktifan dalam persamaan Arrhenius?
di mana k mewakili pemalar kadar, Ea adalah tenaga pengaktifan , R ialah pemalar gas (8.3145 J/K mol), dan T ialah suhu yang dinyatakan dalam Kelvin. A dikenali sebagai faktor kekerapan, mempunyai unit daripada L mol-1 s-1, dan mengambil kira kekerapan tindak balas dan kemungkinan orientasi molekul yang betul.
Berapakah pemalar kadar k?
The pemalar kadar , k , ialah perkadaran tetap yang menunjukkan hubungan antara kepekatan molar bahan tindak balas dan kadar daripada tindak balas kimia. The pemalar kadar boleh didapati secara eksperimen, menggunakan kepekatan molar bahan tindak balas dan susunan tindak balas.
Disyorkan:
Bagaimanakah jururawat menggunakan persamaan linear?

Bidang penjagaan kesihatan, termasuk doktor dan jururawat, sering menggunakan persamaan linear untuk mengira dos perubatan. Persamaan linear juga digunakan untuk menentukan cara ubat yang berbeza boleh berinteraksi antara satu sama lain dan cara menentukan jumlah dos yang betul untuk mengelakkan dos berlebihan dengan pesakit yang menggunakan pelbagai ubat
Bagaimanakah anda menyelesaikan persamaan kuadratik menggunakan undang-undang faktor nol?

Daripada ini kita boleh membuat kesimpulan bahawa: Jika hasil darab mana-mana dua nombor adalah sifar, maka satu atau kedua-dua nombor itu adalah sifar. Iaitu, jika ab = 0, maka a = 0 atau b = 0 (yang termasuk kemungkinan a = b = 0). Ini dipanggil Undang-undang Faktor Null; dan kami sering menggunakannya untuk menyelesaikan persamaan kuadratik
Bagaimanakah anda boleh membuktikan 2 segi tiga serupa menggunakan postulat persamaan SAS sisi sudut sisi?
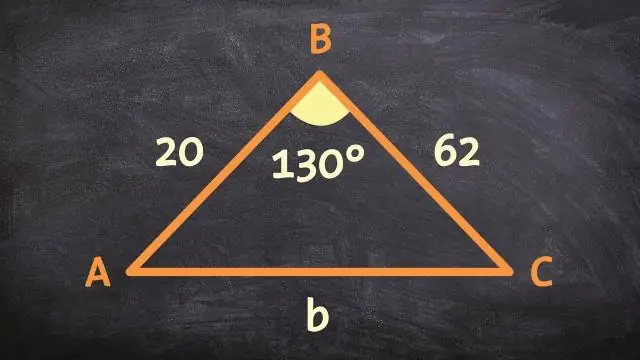
Teorem Persamaan SAS menyatakan bahawa jika dua sisi dalam satu segitiga adalah berkadar dengan dua sisi dalam segitiga lain dan sudut yang disertakan dalam kedua-duanya adalah kongruen, maka kedua-dua segi tiga adalah serupa. Penjelmaan persamaan ialah satu atau lebih penjelmaan tegar diikuti dengan pelebaran
Bilakah anda harus menggunakan korelasi dan bilakah anda harus menggunakan regresi linear mudah?
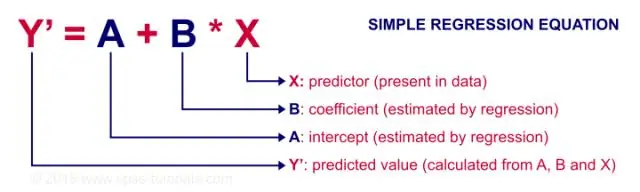
Regresi digunakan terutamanya untuk membina model/persamaan untuk meramalkan tindak balas utama, Y, daripada set pembolehubah peramal (X). Korelasi digunakan terutamanya untuk meringkaskan arah dan kekuatan perhubungan antara satu set 2 atau lebih pembolehubah angka dengan cepat dan ringkas
Bagaimanakah anda menyelesaikan persamaan linear menggunakan penghapusan Gaussian?

Cara Menggunakan Penghapusan Gaussian untuk Menyelesaikan Sistem Persamaan Anda boleh mendarab mana-mana baris dengan pemalar (selain sifar). darab baris tiga dengan –2 untuk memberi anda baris tiga baharu. Anda boleh menukar mana-mana dua baris. menukar baris satu dan dua. Anda boleh menambah dua baris bersama-sama. menambah baris satu dan dua dan menulisnya dalam baris dua
