
- Pengarang Miles Stephen stephen@answers-science.com.
- Public 2023-12-15 23:39.
- Diubah suai terakhir 2025-01-22 17:06.
Peranan daya antara molekul
Kuasa ini mesti terganggu apabila a bahan cair , yang memerlukan input tenaga. Input tenaga diterjemahkan kepada suhu tinggi. Jadi, semakin kuat kuasa-kuasa yang menyatukan pepejal, maka lebih tinggi itu takat lebur.
Tambahan pula, apakah takat lebur bahan tulen?
Takat lebur , suhu di mana pepejal dan cecair membentuk a bahan tulen boleh wujud dalam keseimbangan. Apabila haba digunakan pada pepejal, ia suhu akan meningkat sehingga takat lebur dicapai.
Kedua, mengapa menambah kekotoran menurunkan takat lebur? kekotoran dalam pepejal biasanya lebih rendah yang takat lebur kerana ia mengganggu kekisi kristal murni. Menambah kekotoran kepada cecair biasanya menaikkan mendidih titik kerana peningkatan entropi fasa larutan. Atau anda boleh memikirkan kekotoran sebagai menurunkan tekanan wap cecair.
Kemudian, apakah yang menyebabkan takat lebur lebih tinggi daripada nilai literatur?
Sebatian organik tulen biasanya cair dalam julat dua darjah atau kurang. Sampel adalah najis jika ia mempunyai a takat lebur julat yang lebih rendah dan/atau lebih luas daripada bahawa nilai sastera . Lebih banyak kekotoran meningkat kesan ini.
Mengapakah bendasing menjejaskan takat lebur?
kekotoran dalam sebab yang kukuh a takat lebur kemurungan kerana kekotoran mengganggu tenaga kekisi kristal. Lebih pekat zat terlarut, lebih besar gangguan dan lebih rendah pembekuan titik daripada penyelesaian. Konsep ini boleh digunakan untuk takat lebur (atau beku titik ) daripada sebatian tulen.
Disyorkan:
Mengapakah air mempunyai takat lebur yang tinggi?
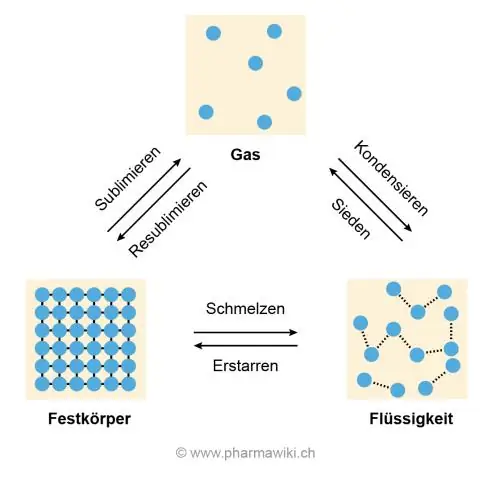
Punca suhu lebur dan pendidihan yang tinggi ialah ikatan hidrogen antara molekul air yang menyebabkan molekul air melekat dan tidak boleh ditarik iaitu apa yang berlaku apabila ais mencair dan air mendidih menjadi gas
Jenis ikatan yang manakah merupakan ciri bagi bahan yang mempunyai takat lebur yang tinggi?

Kekisi ionik Semua sebatian ionik mempunyai takat lebur dan takat didih yang tinggi kerana banyak ikatan ion yang kuat perlu dipecahkan. Mereka mengalir apabila cair atau dalam larutan kerana ion bebas untuk bergerak. Mereka boleh dipecahkan oleh elektrolisis. Mereka biasanya larut dalam air
Mengapakah Aluminium mempunyai takat lebur yang lebih tinggi daripada natrium?

Sepanjang tempoh itu, valensi meningkat (daripada valensi 1 dalam natrium kepada valensi 3 dalam aluminium) supaya atom logam boleh menyahlokasi lebih banyak elektron untuk membentuk lebih banyak kation bercas positif dan lautan elektron terdelokalisasi yang lebih besar. Oleh itu ikatan logam menjadi lebih kuat dan takat lebur meningkat daripada natrium kepada aluminium
Bolehkah dua sebatian tulen mempunyai takat lebur yang sama?

Tiada dua sebatian tulen boleh mempunyai takat lebur yang sama. Dua sebatian tulen boleh mempunyai takat lebur yang sama. Satu contoh ditunjukkan dalam jadual 1.1 di mana takat lebur untuk m-toluamide dan Methyl-4-nitro benzoate adalah betul-betul sama (94-96 ºC)
Mengapakah air mempunyai takat didih dan takat lebur yang tinggi?

Punca suhu lebur dan pendidihan yang tinggi ialah ikatan hidrogen antara molekul air yang menyebabkan molekul air melekat dan tidak boleh ditarik iaitu apa yang berlaku apabila ais mencair dan air mendidih menjadi gas
